Bitte Warten
Das Laden der Strukturdaten dauert einen Augenblick. Bitte haben Sie etwas Geduld!
0 von 0 Strukturen wurden bereits geladen.
Es ist aber wahrscheinlich, dass sich beim Umzug doch das ein oder andere Problem eingeschlichen hat. Bitte meldet Probleme inkl. möglicht genauer Beschreibung und evtl. eines Screenshots an Klaus Schaper.
Animation der Konformationen im Cyclohexan
Studienfach:
Alle_Veranstaltungen
Lernziel
Die Studierenden sollen die wesentlichen Konformationen des Cyclohexans (Sessel, Twist und Wanne) in den verschiedenen Darstellungen erkennen, unterscheiden und zeichnen können! Besondere Aufmerksamkeit soll dabei gelegt werden auf:
- die unterschiedlichen Symmetrieebenen der einzelnen Konformationen,
- die Orientierung der Wasserstoffatome im Raum und zueinander,
- die daraus resultierenden Wechselwirkungen.
Zur Vorbereitung auf die Einheit sind die Module zur Konformation des Ethans und des Butans sehr gut geeignet.
Einleitung
Cyclohexan ist ein cyclischer gesättigter
Kohlenwasserstoff mit der Summeformel C6H12.
Die Atome des Cyclohexanringes sind anders als die erste Vermutung
nahe legt (Abbildung: 1) nicht planar in einer Ebene angeordnet
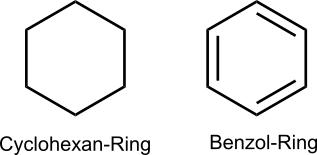 , sondern das Molekül
ist gewinkelt. Die Valenzwinkel zwischen den Kohlenstoffatomen betragen
statt der 120° eines Benzolrings nur 111,4°. Das entspricht fast einem Tetraederwinkel
von 109,5°. Auf diese Weise wird
die
, sondern das Molekül
ist gewinkelt. Die Valenzwinkel zwischen den Kohlenstoffatomen betragen
statt der 120° eines Benzolrings nur 111,4°. Das entspricht fast einem Tetraederwinkel
von 109,5°. Auf diese Weise wird
die  Ringspannung
Ringspannung
gesenkt
und ekliptische Wechselwirkungen zwischen den
Kohlenstoff-Wasserstoff-Bindungen am Ring verringert.
Ähnlich wie in offenkettigen Aliphaten sind die CH2-Gruppen des
Cyclohexanmoleküls beweglich. Zwar ist aufgrund der Ringstruktur keine Rotation
möglich, aber die Methylengruppen nehmen dennoch unterschiedliche Orientierungen
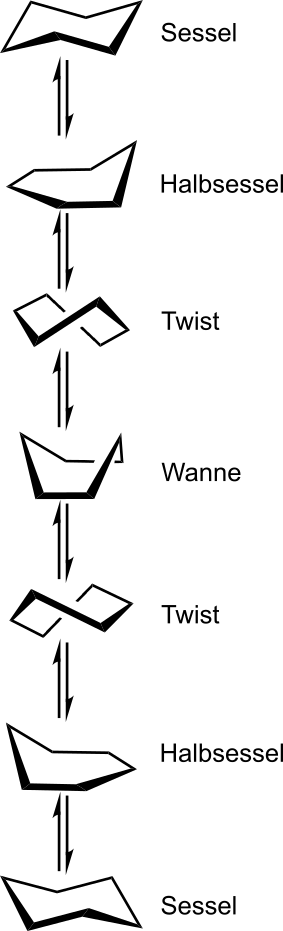
im Raum ein (Abbildung: rechte Spalte). Die eingenommenen Konformationen unterscheiden
sich in ihrer charakteristischen Form und dem jeweiligen Energiegehalt voneinander. Die
Energiebarriere zwischen den einzelnen Isomeren ist so klein, dass Cyclohexanmoleküle
bei Raumtemperatur ständig die Konformation ändern können. Bei tiefen Temperaturen wird die Isomerisierung
dagegen so sehr verlangsamt, dass die einzelnen Konformationen nebeneinander nachweisbar sind. Man unterscheidet
im Wesentlichen die Sessel-, Twist- und Wannenkonformation voneinander.
- Klicken Sie nun zur Bearbeitung des Moduls auf den Start-Button, um das Textfeld und das Animationfeld korrekt auszurichten. Mit Hilfe der Pfeile links und rechts lassen sich die einzelnen Kapitel weiter- bzw. zurückblättern, oder über die Kapitel-Button direkt erreichen.
- Blauer Text entspricht Arbeitsanweisungen, kursive Textzeilen stellen Hilfestellungen und praktische Erklärungen zur Benutzung des Moduls dar, Zusammenfassungen und Merksätze sind in grau gekennzeichnet.
Cyclohexan in der Sesselkonformation (1)

Die energetisch günstigste Konformation des Cyclohexan-Moleküls wird, aufgrund der Ähnlichkeit mit einem Liegesessel, als Sesselkonformation bezeichnet. Die Orientierung in der Form eines Sessels ist nahezu vollständig spannungsfrei und die Abstoßungskräfte zwischen den jeweiligen Wasserstoffatomen sind sehr gering.
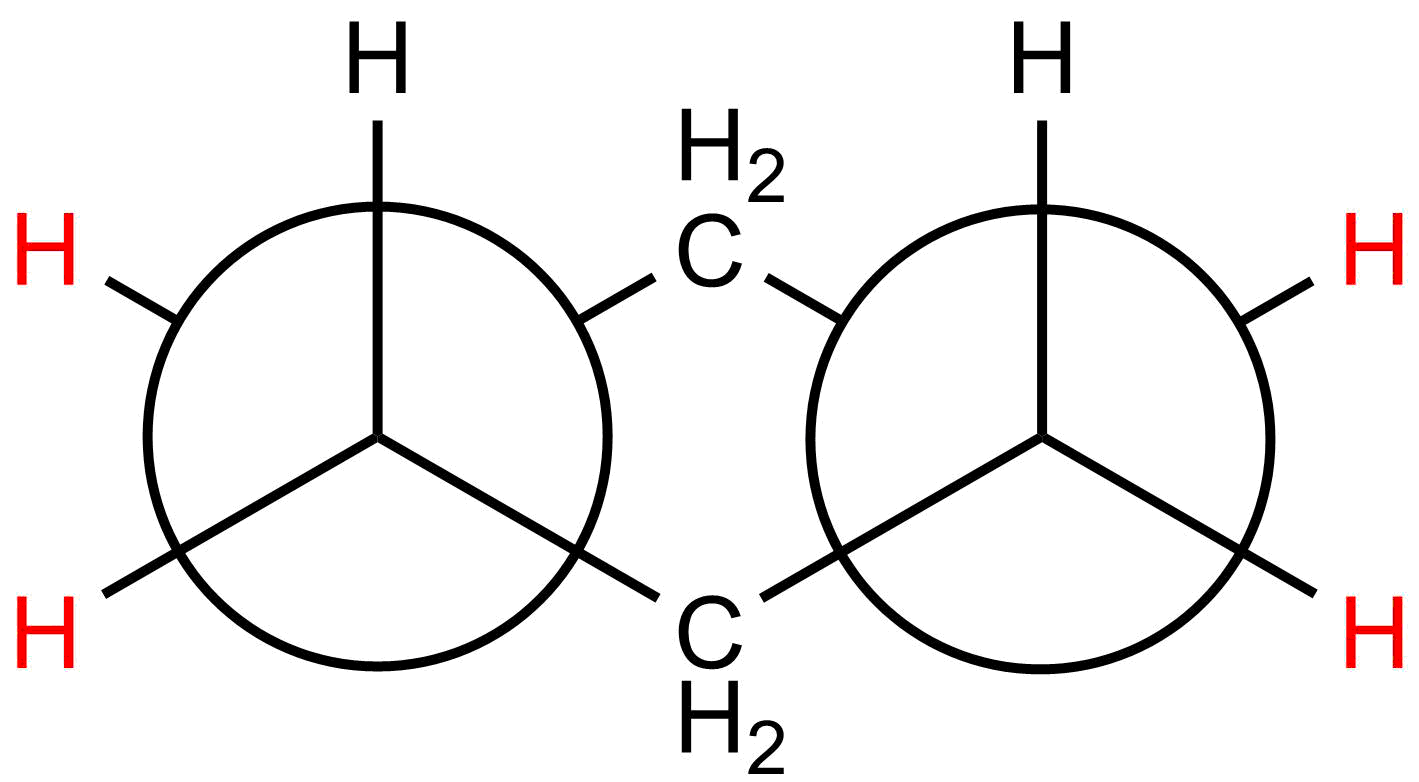 Newman-Projektion von Cyclohexan in gestaffelter Konformation
Newman-Projektion von Cyclohexan in gestaffelter Konformation
Die einzelnen Methylengruppen stehen  gestaffelt
gestaffelt
zu einander (Abbildung rechts), so dass keine sogenannte
 Pitzer-Spannung
Pitzer-Spannung
auftritt. Abstoßende Van-der-Waals-Wechselwirkungen zwischen den Wasserstoffatomen
sind also auf ein Minimum reduziert. Die gestaffelte Orientierung lässt sich leicht durch
Drehen des Moleküls zeigen. Zur besseren Unterscheidbarkeit der Methylengruppen, können diese
unterschiedlich
werden.
- Drehen Sie nun das Molekül so, dass die grüne und orange Methylengruppe hintereinander angeordnet sind. Wenn Sie dies nicht schaffen, dann klicken Sie hier:
- Versuchen Sie jetzt das Molekül um den Uhrzeigersinn zu drehen, so dass die folgenden Methylengruppen gestaffelt angeordnet werden, nutzen Sie die Einfärbung als Hilfe, andernfalls können Sie die entsprechenden Button verwenden: , , , , .
Cyclohexan in der Sesselkonformation (2)

Aus diesem Betrachtungswinkel lässt sich die gestaffelte Anordnung der Wasserstoffatome zueinander gut erkennen. Der zwischen den Atomen beträgt fast 60°, das entspricht dem größtmöglichen Abstand. Bei dieser Ansicht auf das Molekül ist die hohe Symmetrie der Bindungen und Atome gut zu sehen. Zur Verdeutlichung können drei eingeblendet werden. Außerdem kann eine imaginäre durch den Ring gelegt werden. Die Wassestoffatome sind entweder so angeordnet, dass sie in der Ebene liegen oder senkrecht zur Ebene stehen .
Zur weiteren Bearbeitung des Moduls ist es sinnvoll das Animationsfenster neu zu laden. Sie können alternativ auch die nutzen, um die rechte Struktur der linken Struktur gleich anzuordnen.
Cyclohexan und der Halbsessel

Mit Hilfe des Reglers lässt sich die Rotationsgeschwindigkeit einstellen. Die Animation durchläuft alle möglichen Konformationen und beginnt automatisch von neuem. Mit Hilfe der Stop-Button, kann die Animation an einer beliebigen Stelle angehalten bzw. bis zu einer bestimmten Konformation abgespielt werden.
- Starten Sie die Animation im rechten Fenster.
- Stoppen Sie die Rotation, sobald Sie einen Halbsessel (vgl. Abbildung) erkennen können. Alternativ können Sie den entsprechenden Stop-Button verwenden.
- Vergleichen Sie den "Halbsessel" mit der Sesselkonformation im linken Animationsfenster.
Durch Drehung um die C-C-Bindungsachse geht das Molekül in den sogenannten
"Halbsessel" über.
In dieser Anordnung liegen fünf der sechs Kohlenstoffatome fast in einer Ebene.
Die
betragen bis zu 120°, sie sind damit fast so groß wie in einem
Benzolring. Dies führt zu einer stark erhöhten
Ringspannung und erheblichen ekliptischen Wechselwirkungen zwischen den
Methyl-Wasserstoffatomen. Die beiden energiegleichen "Halbsessel" (vgl. Abbbildung oben)
stellen demnach die energiereichste mögliche Anordnung des Cyclohexan-Moleküls
dar und bilden nur einen Übergangszustand zum nächsten Konformer der
Twistkomformation.
Cyclohexan in der Twistkonformation

- Starten Sie die Animation bis sie die 1. Twistkonformation erreichen (Stop-Button).
- Vergleichen Sie den "Twist" (rechts) und "Sessel" (links), überprüfen Sie das rechte Molekül auf Symmetrieelemente.
Die nächste Konformation, die das Cyclohexanmolekül einnimmt ist die Twistkonformation.
Sie bildet einen Übergang zwischen der Anordnung im Sessel und der Wannenkonformation und ähnelt
am ehesten einer stark verdrehten Wanne.
Im Vergleich zum Sesselkonformer ist die Symmetrie der Bindungen verloren gegangen. Die Konformationsänderungen
gegenüber der Halbsesselanordnung sorgen jedoch für eine Abnahme der ekliptischen Wechselwirkungen und eine
deutliche Senkung der  Ringspannung
Ringspannung
Die
betragen durchschnittlich lediglich 112,5°.
Es existieren zwei energiegleiche Twistkonformationen. Sie stellen jeweils ein lokales Minimum im Energieprofil der Konformationsumlagerung dar und verhalten sind spiegelbildlich zueinander. Dies lässt sich u.a. aus der folgenden Ansicht gut nachvollziehen:
- Betrachten Sie die beiden "Twists" aus dieser Ansicht, indem Sie beiden "Stop"-Button zu Hilfe nehmen.
Tipp: Nutzen Sie die Button zur Färbung der Wasserstoffatome, um die Spiegelbilder besser erkennen zu können.
Cyclohexan in der Wannenkonformation

- Untersuchen Sie nun die nächste Konformation, indem Sie die Animation in der Wannenkonformation stoppen (Stop-Button).
Die Wannenkonformation wird eingenommen, indem das Molekül die leichte Verdrehung der Twistanordnungen ausgleicht.
Es entsteht eine Komformation hoher Symmetrie, die einer Wanne oder einem Boot ähnelt. Die ekliptischen Wechselwirkungen
nehmen im Vergleich zu den "Twists" wieder zu. Die ehemals verdrehten Wasserstoffatome stehen in der
nun in einer Reihe. Die Wannenanordnung ist demnach energiereicher als die beiden Twistkonformationen, sie liegt in einem lokalen
Energiemaxium. Es lassen sich gleich
zwei Spiegelebenen durch das Molekül legen.
Cyclohexan in der Sesselkonformation (2)

Über die zweite Twist-Konformation (vgl. Kapitel 4) geht das Cyclohexanmolekül in die 2. Sesselkonformation über. Die beiden Sessel sind energiegleich. Sie lassen sich leicht durch die Anordnung der axialen bzw. äquatorialen Wasserstoffatome unterscheiden.
- Stoppen Sie die Animation des Cyclohexanringes in der 2. Sesselkonformation.
- Nutzen Sie die Button zur Einfärbung der axialen und äquatorialen Wasserstoffatome.
Mit Hilfe der Einfärbung ist zu erkennen, dass die Wasserstoffatome, welche in der ersten Konformation
axial angeordnet sind, nun äquatorial orientiert stehen. Umgekehrt stehen die ursprünglich
äquatorialen Wasserstoffatome jetzt axial. Diese Form der Umlagerung wird auch als
Ringinversion bezeichnet.
Die beiden Sesselkonformere stehen über die bereits behandelten Umlagerungen (Halbsessel, Twist und Wanne)
miteinander im Gleichgewicht. Die Aktivierungsenergie ist so niedrig, dass das Cyclohexanmolekül bei
Raumtemperatur etwa 100.000 mal in der Sekunde zwischen den "Sesseln" wechselt.
Im folgenden Kapitel werden die wesentlichen Charakteristika der einzelnen Konformere zusammengefasst. Anhand eines Energieprofils soll der Energiegehalt der einzelnen Konformere und Übergangszustände eingeordnet werden.
Zusammenfassung
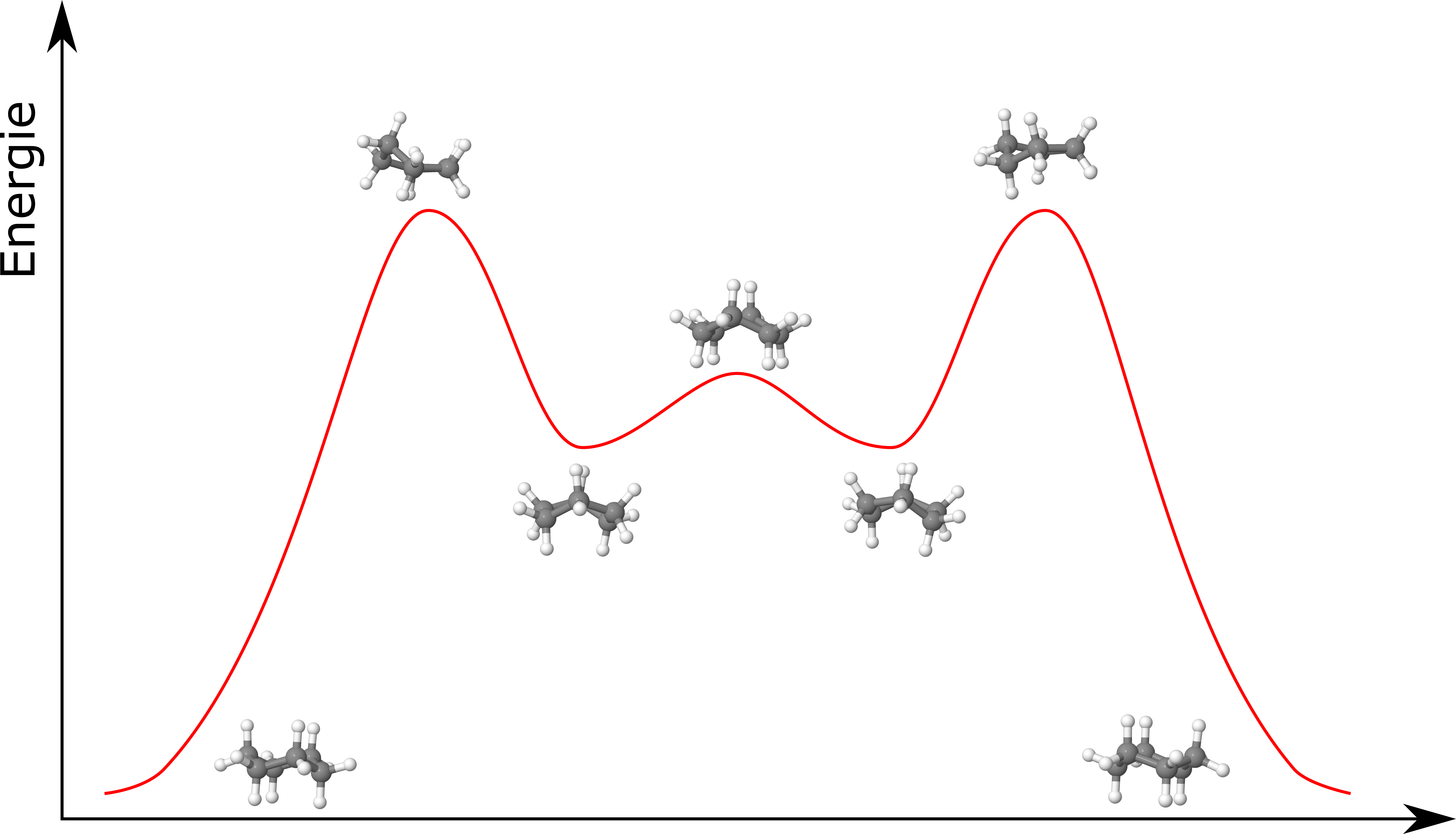
Energieprofil der Konformationsänderungen von Cyclohexan
Das Energieprofil auf der rechten Seite stellt den Energiegehalt der einzelnen Koformationen
relativ zueinander dar. Es ist zu erkennen, dass die Sesselkonformation dem Energieminimum, der
Halbsessel dem Energiemaximum entspricht.
Zusammenfassend lässt sich festhalten, dass das Cyclohexanmolekül während einer
Konformationsumwandlung mehrere Umlagerungen durchläft.
- Die Umlagerung von einer Sesselkonformation in die nächste Sesselkonformation wird als Ringinversion bezeichnet
- Die Umlagerung findet aufgrund der relativ geringen Energiedifferenz zwischen den Konformationszuständen 100.000 mal pro Sekunde statt.
- Es lassen sich Sessel-, Halbsessel-, Twist- und Wannenkonformation unterscheiden.
- Es existieren zwei Sessel-, Halbsessel- und Twistkonformationen, die jeweils energiegleich sind.
- Die beiden Sesselkonformationen lassen sich anhand der Stellung der axialen und äquatorialen Wasserstoffatome unterscheiden.
- Die Sessel- und Twistkonformation bilden der Definition nach Konformere, wobei "Twist" nur metastabil im Vergleich zu "Sessel" ist.
- Halbsessel und Wanne bilden lediglich Übergangszustände, die auch bei tiefen Temperaturen nicht isolierbar sind.
Einfluss von Substituenten am Cyclohexanring
Wie bereits in Kapitel 6 und Kapitel 7 angesprochen, ist der Energiegehalt der Sesselkonformere eines unsubstituierten Cyclohexanrings gleich. Sie unterscheiden sich im Wesentlichen in der Stellung der axialen bzw. äquatorialen Wasserstoffatome.
Der Austausch eines Wasserstoffatoms durch einen anderen Substituenten z.B. einem Halogenatom oder einer Methylgruppe führt dazu, dass sich die beiden Konformationen energetisch unterscheiden. Steht der Substituent axial, treten erhöhte ekliptische Wechselwirkungen im Vergleich zu einem Wasserstoffatom auf. Bei äquatorialer Stellung sind dieser Kräfte geringer, die entsprechende Sesselkonformation ist energieärmer.
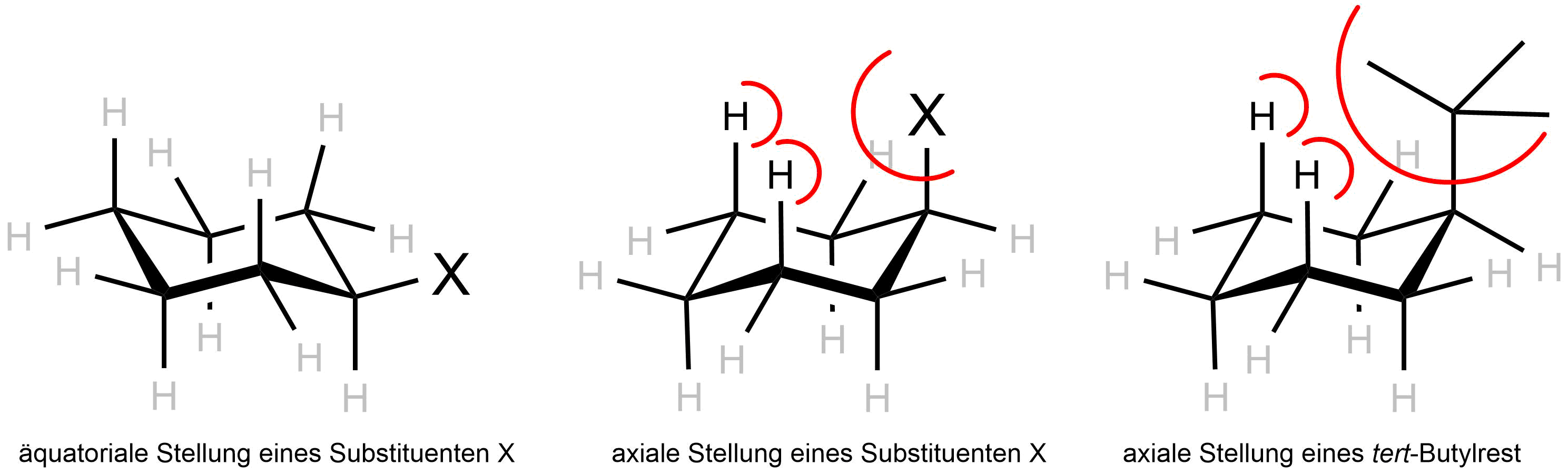
Wechselwirkungen eines Substituenten X in axialer (links) und äquatorialer Stellung
(mitte), sowie die Wechselwirkungen eines tert-Butylrests mit benachbarten Wasserstoffatomen (rechts).
Je sterisch anspruchsvoller der Subsituent ist, desto größer ist der energetische Unterschied zwischen den beiden Sesselkonformeren. Ist die Energiedifferenz groß genug, ändert das Molekül seine Konformation nicht mehr. Man spricht von einem sogenannten Konformationsanker. Der tert-Butylrest ist ein populäres Beispiel für einen Konformationsanker (s. Abbildung oben).
Ausblick
In diesem Modul wurde detailiert auf die Konformationsänderung des Cyclohexanmoleküls eingegangen und der Einfluss von Substituenten angesprochen. In Zukunft sollen weitere Module zum Thema Konformationen entstehen, in denen u.a. genauer auf den Substituenteneinfluss eingegangen werden soll:
- Konformationsänderungen von Methylcyclohexan
- Konformationsänderungen von Dimetyhlcyclohexan
- Konformationsänderungen von t-Butylcyclohexan
- Konformationsänderungen von Decan
- Energiegehalt und Stabilität der Konformationen von Dihalogenalkanen und -alkenen
umlagerungen des Cyclohexanmoleküs
|
Die 3D-Animationen auf dieser Seite wurden mit Hilfe von JSmol erstellt: an open-source Java viewer for chemical structures in 3D. http://www.jmol.org/
scheLM 3D
scheLM Gl
scheLM I4
scheLM IR
scheLM n2s
scheLM NMR
scheLM PSE
scheLM ReRe
scheLM TV
scheLM tys
scheLM Vote
Auszeichnungen Personen Datenschutz Impressum
Wir danken dem eLearning-Förderfonds der Heinrich-Heine-Universität und dem Lehrförderungsfond der Heinrich-Heine-Universität, sowie dem Fellowship Digitale Innovation in der Hochschullehre des Landes Nordrhein-Westfalen, sowie OER-Content.NRW für die Unterstützung.
© Copyright 2013 bis 2025, PD Dr. Klaus Schaper


